مقاله علمی اثر ژل رویال بر سندروم روی تخمدان پلی کیستیک | قسمت اول

عنوان مقاله : مکمل ژل رویال و اثر ضد آندروژنی آن بر پارامترهای تولید مثلی در سندرم تخمدان پلی کستیک (PCOS) در مدل حیوانی
سندروم تخمدان پلی کیستیک (PCOS) رایج ترین اختلال غدد درون ریز در بین زنان است که بر زمان باروری زنان تاثیر می گذارد. شیوع این سندروم در مالزی حدود 12.6% و برای زنان با قومیت های متفاوت در سرتاسر جهان حدود 5-16% تخمین زده شد. معیارهای اجماع روتردام برای تشخیص سندروم بستگی به حضور حداقل دو تا از علایم زیر دارد:
کم بودن میزان تخمک یا فقدان تخمک (اختلال عمل تخمک گذاری) که از ویژگی های هیپراندروژنیسم و تخمدان پلی کیستیک است. تشدید فعالیت اندروژنی یا مازاد آندروژن های گردشی یکی از مهم ترین خصوصیات سندروم تخمدان پلی کیستیک هستند که منجر به بهم خوردگی عملکرد تخمدان و باروری زنان می شود.
مقادیر آندروژن اضافی می تواند پروژسترون تولید شده توسط گنادوتروپین و سنتز استروژن در فولیکول ها (کیسه ای پر از مایع در تخمدان که حاوی تخمک است) را اصلاح کند. در نتیجه منجر به اختلال فیزیکی و فیزیولوژیکی مانند رویش غیرطبیعی مو، ناهنجاری قاعدگی، ناباروری و عدم تحمل گلوکز می شود.
مطالعات همچنان گزارش داده اند که استرس اکسیداتیو ارتباط نزدیکی با ویژگی های پاتولوژیک سندروم دارد و افراد مبتلا به این سندروم عدم تعادل در وضعیت آنتی اکسیدانی دارند. درمان جایگزین هورمونی متعارف برای بیماران سندروم به نظر می رسد تولید عوارض جانبی نامطلوبی مانند التهاب پستان، لکه دارشدن واژن و افزایش فشار خون کند. بنابراین، ارائه و کشف درمان های جایگزین جدید برای عقب انداختن تشدید فعالیت اندروژنی با حداقل عوارض جانبی بسیار مهم است.
ژل رویال یا شیر زنبورعسل توسط غدد تحتانی حنجره زنبورهای عسل کارگر تولید می شود و از یک ماده مترشحه اسیدی سفید مایل به زرد با طعم و بوی کمی تند تشکیل شده است. این ماده یک محصول حیاتی در میان تولیدات زنبورعسل با خواص بیولوژیکی و تغذیه ای بالا در نظر گرفته شده است. به طور کلی ژل رویال از آب (60-70%)، پروتئین (9-18%) قندها (7-18%)، چربی (3-8%)، مواد معدنی، ویتامین ها و اسیدهای آمینه ضروری تشکیل شده است. ژل رویال دارای برخی از خواص بیولوژیکی مانند آنتی باکتریال، ضد سرطان، تنظیم کننده ایمنی و خواص آنتی اکسیدان است.
ژل رویال همچنین علایم یائسگی را بهبود می بخشد، قدرت باروری را افزایش داده، عملکرد تولید مثل را بهبود بخشیده و وضعیت استرس اکسیداتیو در خرگوش های نر را کاهش می دهد. مطالعات نشان داده اند که مصرف ژل رویال باعث افزایش هورمون پروژسترون و میزان بارداری در گوسفندان ماده می شود. همچنین نشان داده شده است که این ژل فعالیت استروژنی را بوسیله کنش واکنش با گیرنده های استروژن تنظیم کرده و بیان ژن های پاسخگو به استروژن را بالا می برد.
10- هیدروکسی- ترانس-2 -دکنوییک اسید، 10- هیدروکسی دکنوییک اسید ، ترانس-2- دکنوییک اسید، و 24- متیلن کلسترول ترکیبات موجود در ژل رویال هستند و به عنوان کارامدترین آزمایش های پیوند لیگاند برای گیرنده های استروژن شناسایی شده اند. تا به امروز، هیچ مطالعه ای در مورد اثرات احتمالی ضد آنروژنی ژل رویال بر پارمتر های تولید مثل در یک مدل حیوانی دارای سندروم انجام نشده است. بنابراین، در مطالعه کنونی، ما مقادیر مصرف مختلف ژل رویال را برای هرگونه اثر بر پروفایل هورمونی، چرخه استروس ( دوره متناوب در حیوانات ماده )، وضعیت اکسیدانی- آنتی اکسیدانی و تاریخ شناسی تخمدان در رابطه با وجود ترکیبات گیاهی شیمیایی و فعال زیستی آن را مورد ارزیابی قرار داده ایم.
مواد و روش های به کار رفته در این آزمایش
در ادامه به مواد و روش هایی که در این آزمایش برای بررسی اثرگذاری ژل رویال بر روی درمان تخمدان پلی کیستیک در مدل های حیوانی پرداخته شده است.
ژل رویال
ژل رویال از زنبور عسل (Apis mellifera) از یک زنبوردار محلی در جوهور ، مالزی خریداری شد. ژل رویال در طی فوریه تا ژوئن (فصل خشک) جمع آوری و در دمای منفی 80 درجه سانتیگراد نگهداری شد. بر اساس روش عادی سازی ناحیه سطح بدن، مقدار مصرف ژل رویال (100 میلی گرم / کیلوگرم در موش صحرایی) برای مطالعه حیوانی متناسب با مقدار ژل رویال تازه مصرف شده به طور سنتی در انسان ها بود که 1 گرم بر کیلوگرم وزن بدن است. بنابراین، مقدار مصرف استفاده شده در مطالعه حاضر، 100 میلی گرم / کیلوگرم (به عنوان یک دوز کم)، 200 میلی گرم / کیلوگرم ( به عنوان یک دوز متوسط) و 400 میلی گرم / کیلوگرم ( به عنوان یک دوز بالا ) بود. ژل رویال با تعلیق آن در آب مقطر برای ایجاد سوسپانسیون 5/0 میلی لیتر تازه تهیه شد و سپس توسط گاواژ خوراکی به موش ها تجویز شد.
غربالگری فیتوشیمیایی و کروماتوگرافی مایع- تجزیه تحلیل طیف سنجی جرمی
آزمایش غربالگری فیتوشیمیایی با استفاده از روش های استاندارد قبلی برای ارزیابی وجود آلکالوئیدها، فنل ها، فلاونوئیدها، گلیکوزیدها، رزین ها، ساپونین ها، تانن ها، ترپنوئیدها و گزانتوپروتئین ها انجام شد. تجزیه و تحلیل کروماتوگرافی مایع و طیف سنجی جرمی برای آنالیز حضور ترکیبات فیتوشیمیایی غیر فرار انجام شد. این کار با استفاده از بررسی کننده فینگان به علاوه ابزار HPLC (Shimadzu-Hitachi, Kyoto, Japan) تجهیز شده با یک ردیاب آرایه دیودی (DAD) اجرا شد و با یک MSجفت شد.
سیستم کروماتوگرافی متشکل از پمپ کواترنر، نمونه گیرخودکار، گازگیر، آشکارساز آرایه فوتودیود و محفظه ستون ترموستاتیک اتوماتیک بود. در مجموع 10 میلی گرم ژل رویال از طریق یک غشای نایلونی 2/0 میکرومتر با سرعت 1 میلی لیتر در دقیقه فیلتر شد، سپس 200 میکرولیتر / دقیقه در طیف سنج جرمی از هم جدا شد. این آزمایش با استفاده از هلیوم به عنوان گاز برخورد با سرعت انرژی 25- 40eV انجام شد. طیف های جرمی حداکثر برای جرم هر یک از یون های هر بار (m/z) در مورد اسامی مرکب احتمالی در محدوده 200-600 نانومتر بدست آمد و شناسایی ترکیبات با استفاده از ReSPect انجام شد ( پایگاه داده طیفی RIKEN MSn برای مواد گیاهی شیمیایی ، یوکوهاما ، ژاپن).
طراحی تجربی حیوانات
چهل موش ماده نابالغ Sprague Dawley (40 تا 50 گرم؛ 3 هفته متولد شده ) از دانشگاه مرکز تحقیقات و خدمات حیوانات ساینز مالزی دریافت شدند. سازگاری برای تمام موش ها به مدت حداقل 4 روز در آزمایشگاه قبل از آزمایش مجاز بود. موش ها تحت دمای محیط (22± 2 درجه سانتی گراد) با چرخه نور روشن/تاریک 12:12 ساعت نگهداری می شدند، آب به مقدار کافی فراهم می شد و از یک رژیم غذایی موش صحرایی تجارتی تغذیه می شدند. این موش های صحرایی به روش تصادفی سازی ساده به دو گروه کنترل (8 موش سالم معمولی ) و تحت درمان تستوسترون (32 تا) تقسیم شدند. افزایش آندروژن در گروه تحت درمان تستوسترون با تزریق روزانه زیر جلدی پروپیونات T در روغن زیتون (10 میلی گرم / کیلوگرم) به مدت 3 هفته القا شد در حالی که گروه کنترل مقدار مساوی از روغن زیتون به همان شکل دریافت کردند. پس از 3 هفته، حیوانات هر گروه به مدت 4 هفته به صورت روزانه تحت درمان قرار گرفتند مطابق با آنچه در پایین آمده است:
الف ) گروه کنترل : روغن زیتون زیرپوستی (10 میلی گرم / کیلوگرم وزن بدن ) و آب مقطر خوراکی (5/0 میلی لیتر) داده شد ؛
ب ) گروه تستوسترون : تستوسترون زیرپوستی و آب مقطر خوراکی داده شد ؛
ج ) گروه تستوسترون 100 ژل رویال : تستوسترون زیرپوستی و ژل رویال 100 میلی گرم / کیلوگرم وزن بدن خوراکی داده شد ؛
د ) گروه تستوسترون 200 ژل رویال : تستوسترون زیرپوستی و ژل رویال 200 میلی گرم / کیلوگرم وزن بدن خوراکی داده شد ؛
ه ) گروه تستوسترون 400 ژل رویال : تستوسترون زیرپوستی و ژل رویال 400 میلی گرم / کیلوگرم وزن بدن خوراکی داده شد.
در پایان دوره آزمایشی، این حیوانات طی 1 شبانه روز تغذیه نشده و به صورت داخل صفاقی با 190 میلی گرم /کیلوگرم کتامین و 5 میلی گرم /کیلوگرم اگزیلازین در طول مرحله دو دوره ای متناوب حیوان ماده بیهوش شدند. موش ها قربانی شده و خون از طریق بزرگ سیاهرگ خلفی برای تعیین هورمون های زایشی جمع آوری شد. تخمدان برای تعیین وضعیت اکسیدان / آنتی اکسیدان و ارزیابی بافت شناختی برش برداری شد. آزمایش این حیوانات مطابق با راهنمای مراقبت و استفاده از حیوانات آزمایشگاهی دانشگاه ساینز مالزی هدایت شده و این مطالعه بوسیله کمیته اخلاقی حیوانات دانشگاه ساینز مالزی مورد تایید قرار گرفته است.
اندازه گیری هورمون های زایشی
نمونه خونی سانتریفوژ شد و سرم جدا شده برای تعیین هورمون های زایشی مورد استفاده قرار گرفت. مقادیر ( تستوسترون، استرادیول، هورمون لوتینیزینگ، و FSH با استفاده از جعبه ابزارهای موجود تجارتی.
ارزیابی چرخه استروس (مرحله دوره ای متناوب حیوان ماده)
درطول درمان، چرخه استروس به صورت روزانه توسط فروتی ( گسترش ) مهبلی به مدت 4 هفته هر روز صبح بین 9 و 10 شب ارزیابی شد. میزان کمی از آب نمک نرمال 9 درصد در داخل ورودی مجرای مهبلی بکار رفت و به ملایمت بیرون زده شد. سوسپانسیون روی یک اسلاید شیشه ای با استفاده از یک درپوش قطره چکان شیشه ای با نوک کند شده قرارداده شد تا وجود لوکوسیت ها، سلول های اپی تلیال میخچه ای شده و سلول های اپی تلیال هسته دار شده ارزیابی شوند. اسلاید با جابجایی کاور بسته شده و با بزرگ نمایی های 10 برابر و 40 برابر تحت یک میکروسکوپ نوری بررسی شدند. ارزیابی چرخه استروس براساس نسبت سلول ها تعیین شد.
اندازه گیری وضعیت اکسیدان – آنتی اکسیدان
تخمدان سمت راست برداشته شد، با آب نمک نرمال سرد شده با یخ شستشو شده و بلافاصله با آب نمک بافرشده با فسفات هموژنیزه شد. پس از سانتریفوژ شدن با 4000 دور در دقیقه به مدت 15 دقیقه، ماده شناور جمع آوری شده و در دمای 80- درجه سانتی گراد تا استفاده بعدی برای آنالیز وضعیت اکسیدان – آنتی اکسیدان (مالون دی الدئید)، ظرفیت آنتی اکسیدان کامل، دی اسموتاز، پراکسیداز گلوتاتیون، و کاتالاز با استفاده از جعبه ابزارهای موجود تجارتی ذخیره شد.
بافت شناسی تخمدان
تخمدان سمت چپ به دقت برش برداری شده و در 10 % فرمالین ثابت نگه داشته شد. این تخمدان به بخش های کوچک تقسیم شده، پردازش شد و با هماتوکسیلین و ائوزین رنگ آمیزی شد. ارزیابی بافت شناختی تخمدان براساس تعداد فولیکول های کیستی ( بیش از 12 کیست به صورت آنرمال درنظرگرفته شدند) و حضور فولیکول های اولیه، فولیکول های ثانویه و اجسام زرد قرارداشت. این بخش در زیر یک آنالیزر تصویربرداری با بزرگ نمایی 40 برابر بررسی شد.
آنالیز آماری
همه داده های بدست آمده با استفاده از نرم افزار IBM SPSS نسخه 22 آنالیز آماری شدند. انتشار و واریانس داده های رقمی به ترتیب با استفاده از پلات whisker-box و تست Levene ارزیابی شدند. داده های با انتشار نرمال و واریانس همگون با استفاده از آنالیز واریانس یک طرفه ANOVA و متعاقبش تست Tukey’s post-hoc بررسی شده و به عنوان میانه ارایه شدند. داده های مقوله ای با استفاده از تست های Pearson’s chi-squared یا تست های دقیق فیشر آنالیز شده و به صورت درصدها ارایه می شوند. یک مقدار p < 0.05 از نظر آماری معنی دار در نظرگرفته شد.
نتایج آزمایش حیوانی برای مشخص شدن اثر ژل رویال بر درمان تخمدان پلی کیستیک
این نتایج در چند دسته ارائه شده اند:
* غربالگری فیتوشیمیایی و کروماتوگرافی مایع- تجزیه تحلیل طیف سنجی جرمی
آزمایش غربالگری فیتوشیمیایی هر 9 ماده مرکب فیتوشیمیایی یافت شده در ژل رویال همراه با فعالیت های زیستی گزارش شده شان را آشکار کرد. از آنالیز LC–MS ، ما 12 ماده مرکب غیر فرار فیتوشیمیایی یافت شده در ژل رویال را شناسایی کردیم و فعالیت های زیستی گزارش شده شان در جدول 2 ارایه شده اند. ماده مرکب با بالاترین طیف جرمی ادنوزین– 5- مونوفسفات بود(348 m/z)، درحالی که اسید سباسیک (185 m/z) دارای کمترین طیف جرمی بود. کروماتوگرام و تخصیص های حداکثر مواد مرکب در شکل 1 نشان داده شده اند.
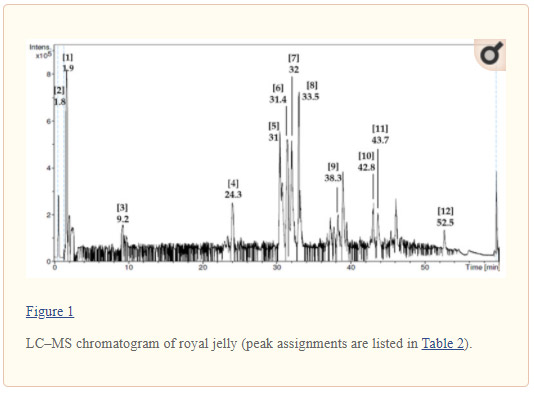
اثر ژل رویال بر تخمدان پلی کیستیک » شکل ( 1 )
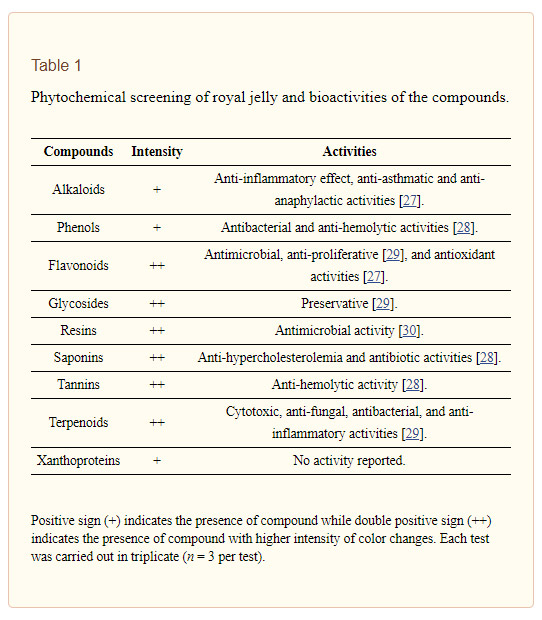
داده های در مورد تخمدان پلیکیستیک » جدول ( 1 )
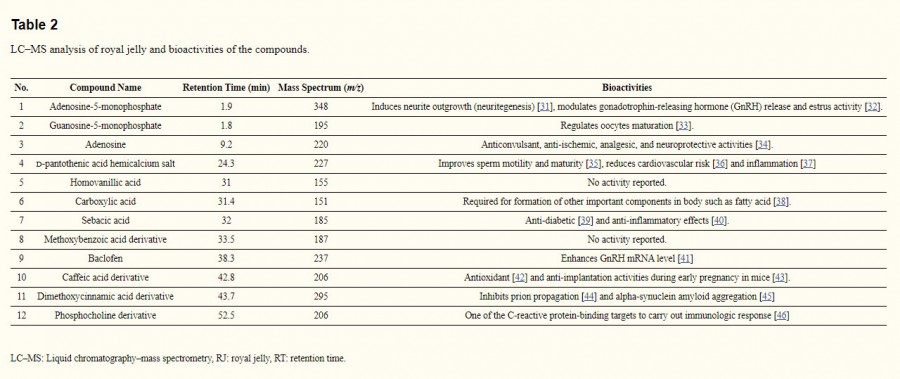
اطلاعات در مورد درمان تخمدان پلی کیستیک سندروم » جدول ( 2 )
اثر ژل رویال بر بافت شناختی تخمدان در موش های دارای سندرم PCOS
تخمدان گروه کنترل رشدهای فولیکولار نرمال گسترش های فولیکولی نرمال با حضور فولیکول های اولیه، فولیکول های ثانویه و اجسام زرد نشان داد. پس از تحریک شدن با تستوسترون ( گروه تی )، در درون تخمدان فولیکول کیستی بزرگ با آستر سلولی پوشش و سلول های گرانولوزای نازک جای داده شد. شکل 2 قسمت C وجود فولیکول های کیستی پس از درمان با مقدار کم ژل رویال ( گروه تستوسترون 100 ژل رویال) را فاش می کند. مشاهده بافت شناختی در گروه تستوسترون 200 ژل رویال، بازیابی بافت تخمدان با مراحل مختلف رشد فولیکولی شامل جسم زرد، فولیکول های اولیه و فولیکول های ثانویه را نشان داد و کیست ها عمدتاً ناپدید شدند. درضمن، در گروه تستوسترون 400 ژل رویال، تخمدان دارای تعداد کاهش یافته ای از جسم زرد، و اندازه کوچک شده ای از فولیکول های کیستی بود.
از آنالیز کمیتی، معلوم شد که:
* تعداد فولیکول های اولیه به طرز چشمگیری بیشتر در گروه های تستوسترون، تستوسترون 100 ژل رویال و تستوسترون 400 ژل رویال در مقایسه با گروه کنترل بود. در گروه تستوسترون 200 ژل رویال این تعداد فولیکول ها به طرز چشمگیری در مقایسه با گروه های تستوسترون و تستوسترون 100 ژل رویال کمتر بود، اما مشابه به گروه کنترل بود. به هرحال، تعداد فولیکول های اولیه به طرز چشمگیری بیشتر در گروه تستوسترون 400 ژل رویال در مقایسه با گروه تستوسترون 200 ژل رویال بود.
* همچنین تعداد فولیکول های ثانویه به طرز چشمگیری در گروه های تستوسترون، تستوسترون 100 ژل رویال و تستوسترون 400 ژل رویال در مقایسه با گروه کنترل کمتر بود. علاوه بر این، در گروه تستوسترون 200 ژل رویال، تعداد فولیکول های ثانویه به طور قابل ملاحظه ای در مقایسه با گروه های تستوسترون و تستوسترون 100 ژل رویال بالاتر بود. ضمناً، تعداد فولیکول های ثانویه به طور قابل ملاحظه ای در گروه تستوسترون 400 ژل رویال در مقایسه با گروه تستوسترون 200 ژل رویال کمتر بود.
* تعداد جسم زرد به طور قابل ملاحظه ای در گروه های تستوسترون و تستوسترون 400 ژل رویال در مقایسه با گروه کنترل کمتر بود. این تعداد جسم زرد به طور قابل ملاحظه ای در گروه های تستوسترون 100 ژل رویال و تستوسترون 200 ژل رویال در مقایسه با گروه تستوسترون بالاتر بود. گروه تستوسترون 200 ژل رویال همچنین دارای تعداد جسم زرد به طور قابل ملاحظه بالاتری در مقایسه با گروه های تستوسترون 100 ژل رویال و تستوسترون 400 ژل رویال بود.
* تعداد فولیکول های کیستی به طور قابل ملاحظه ای درگروه های تستوسترون 100 ژل رویال و تستوسترون 400 ژل رویال در مقایسه با گروه کنترل بالاتر بود. ضمناً ، تعداد فولیکول های کیستی به طور قابل ملاحظه ای در گروه های تستوسترون 100 ژل رویال، تستوسترون 200 ژل رویال و تستوسترون 400 ژل رویال در مقایسه با گروه تستوسترون کمتر بود. تعداد فولیکول های کیستی هم به طور قابل ملاحظه ای در گروه تستوسترون 200 ژل رویال در مقایسه با گروه تستوسترون 100 ژل رویال کمتر بود، اما مشابه به گروه کنترل بود.
اثر ژل رویال بر سندروم روی تخمدان پلی کیستیک | قسمت دوم
از طریق لینک زیر می توانید مقاله کامل به صورت لاتین را مطالعه نمایید:
www.ncbi.nlm.nih.gov/pmc/articles/PMC7346114
اطلاعات شناسنامه ای مقاله:
PMCID: PMC7346114
PMID: 32517356
doi: 10.3390/antiox9060499









